07/12/2015
En el corazón de toda la materia, desde la sal común en tu mesa hasta los intrincados componentes de tu ADN, se encuentra un principio fundamental: los enlaces químicos. Estas uniones invisibles son las que dictan cómo los átomos se agrupan para formar moléculas y estructuras más complejas. Pero, ¿alguna vez te has preguntado por qué algunos materiales son duros y cristalinos, mientras que otros son gases volátiles o líquidos conductores? La respuesta reside en el tipo de "acuerdo" que los electrones establecen entre los átomos. Hoy, nos adentraremos en el intrigante mundo del enlace iónico, explorando su naturaleza, sus diferencias con otros enlaces vitales como el covalente y el metálico, y cómo estas interacciones fundamentales moldean las propiedades de todo lo que conocemos.
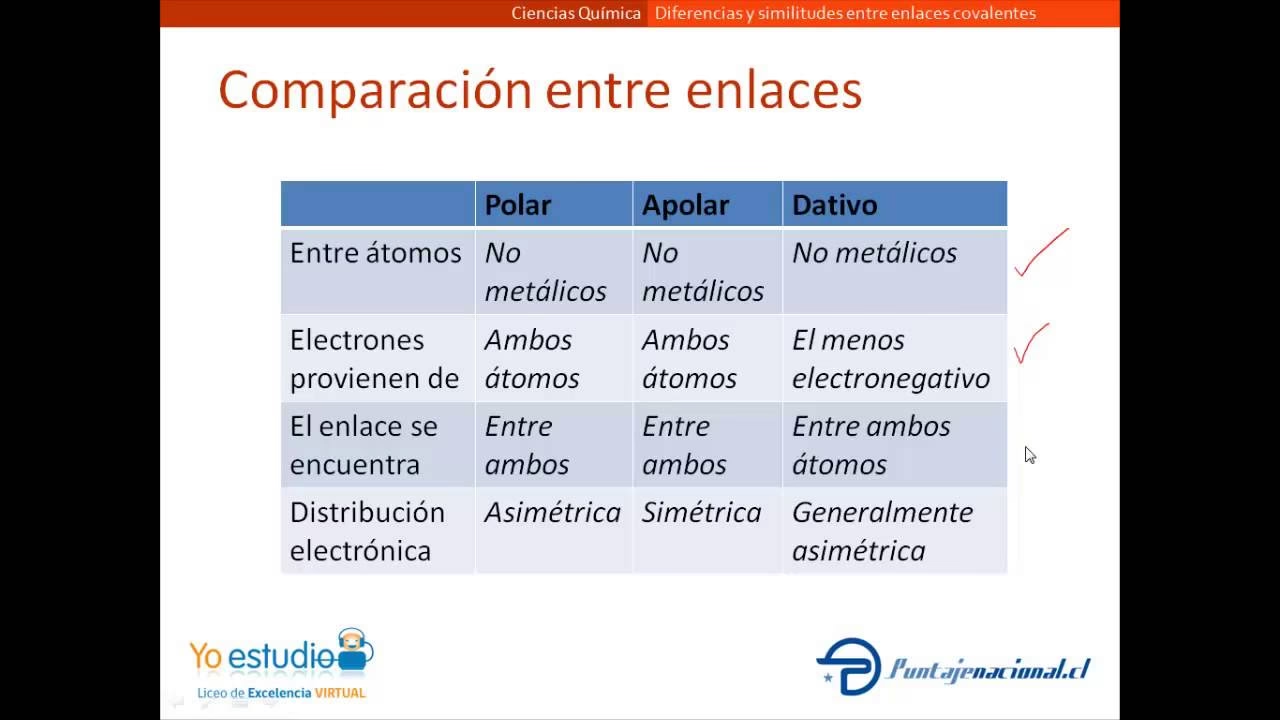
Imagina los átomos como pequeños individuos con una cantidad de electrones que desean estabilidad. Para lograr esa estabilidad, comparable a tener la "órbita" de electrones completa, los átomos pueden optar por diferentes estrategias: ceder, aceptar o compartir electrones. Estas estrategias son la base de los distintos tipos de enlaces químicos. Comprender estas dinámicas electrónicas no solo es crucial para la química, sino que también nos permite apreciar la profunda interconexión entre la estructura a nivel atómico y las propiedades macroscópicas de los materiales.
- ¿Qué es un Enlace Iónico? La Transferencia Electrónica
- El Contraste Fundamental: Iónico vs. Covalente
- Más Allá del Iónico y Covalente: El Enlace Metálico
- Impacto en las Propiedades de la Materia
- Preguntas Frecuentes sobre Enlaces Químicos
- ¿Qué significa que un enlace sea iónico?
- ¿Cuál es la diferencia principal entre un enlace iónico y uno covalente?
- ¿Entre qué tipos de átomos se forman los enlaces iónicos?
- ¿Los compuestos iónicos conducen la electricidad?
- ¿Qué diferencia hay entre un enlace iónico y uno metálico?
- ¿Por qué los compuestos iónicos tienen altos puntos de fusión?
¿Qué es un Enlace Iónico? La Transferencia Electrónica
Cuando hablamos de que algo es iónico, nos referimos a un tipo particular de enlace químico que se forma mediante la poderosa atracción electrostática entre iones de carga opuesta. Para que esto ocurra, debe haber una transferencia completa de uno o más electrones de un átomo a otro. Piensa en ello como una transacción de electrones: un átomo, generalmente un metal, tiene una baja afinidad por sus electrones más externos y está dispuesto a cederlos. Al perder electrones, este átomo se convierte en un ion con carga positiva, conocido como catión (por ejemplo, Na+).
Por otro lado, hay un átomo, generalmente un no metal, que tiene una alta afinidad por los electrones y está ansioso por aceptarlos para completar su propia capa externa. Al ganar electrones, este átomo se transforma en un ion con carga negativa, llamado anión (por ejemplo, Cl-). Una vez que estos iones con cargas opuestas se han formado, se atraen mutuamente con una fuerza considerable, similar a la atracción entre los polos opuestos de un imán. Esta fuerte atracción electrostática es lo que constituye el enlace iónico.
Un ejemplo clásico y fácil de visualizar es el cloruro de sodio (NaCl), la sal de mesa. El sodio (Na) es un metal alcalino con un electrón en su última capa, mientras que el cloro (Cl) es un halógeno con siete electrones en su capa externa. El sodio cede su electrón al cloro, resultando en un ion Na+ y un ion Cl-. Estos iones se unen fuertemente para formar una estructura cristalina, que es la razón por la que la sal es un sólido duro y quebradizo a temperatura ambiente.
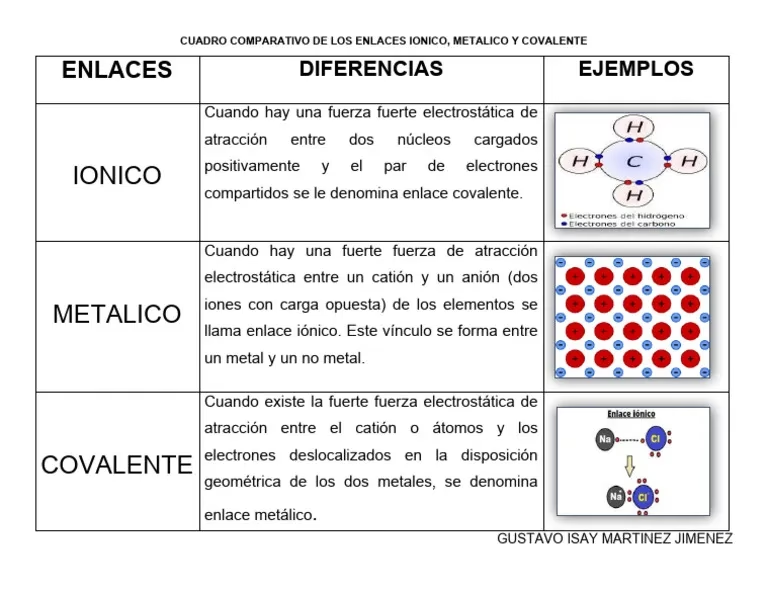
El Contraste Fundamental: Iónico vs. Covalente
Aunque los enlaces iónicos son fundamentales, no son el único tipo de unión química. El otro protagonista principal es el enlace covalente, y la diferencia entre ambos es crucial para entender la diversidad de la materia. Mientras que el enlace iónico se basa en la transferencia total de electrones, el enlace covalente se fundamenta en la compartición de uno o más pares de electrones entre dos átomos.
Imagina a los átomos en un enlace covalente como dos amigos que deciden compartir un juguete: ambos lo necesitan, y al compartirlo, ambos se benefician. Esta compartición de electrones ocurre generalmente entre átomos de elementos con electronegatividades similares, lo que significa que ninguno de los átomos es lo suficientemente fuerte como para arrebatarle los electrones al otro. Esto permite que los electrones se muevan entre ambos átomos, creando una unión estable. El agua (H2O) es un excelente ejemplo de un compuesto con enlaces covalentes, donde los átomos de hidrógeno comparten electrones con el oxígeno.
Tabla Comparativa: Enlace Iónico vs. Enlace Covalente
| Característica | Enlace Iónico | Enlace Covalente |
|---|---|---|
| Naturaleza de los Electrones | Transferencia completa de electrones de un átomo a otro. | Compartición de uno o más pares de electrones entre dos átomos. |
| Átomos Involucrados | Generalmente entre metal y no metal (gran diferencia de electronegatividad). | Generalmente entre no metales (electronegatividades similares). |
| Formación de Iones | Sí, se forman cationes y aniones. | No, no se forman iones discretos. |
| Estructura Típica | Redes cristalinas sólidas (iones ordenados). | Moléculas discretas o redes covalentes (estructuras continuas). |
| Puntos de Fusión/Ebullición | Generalmente altos. | Generalmente bajos (en moléculas discretas), muy altos (en redes covalentes). |
| Conductividad Eléctrica | Conductores en estado fundido o en solución acuosa; aislantes en estado sólido. | La mayoría no conduce electricidad en ninguna fase. |
| Solubilidad en Agua | Alta solubilidad en disolventes polares como el agua. | Varía; las moléculas polares son solubles, las apolares no. |
| Dureza y Fragilidad | Duros y frágiles. | Varían; desde gases blandos hasta sólidos muy duros. |
La diferencia en la naturaleza de los electrones compartidos o transferidos es la clave. En un enlace iónico, los electrones son esencialmente "donados" y "aceptados", creando entidades cargadas que se atraen. En un enlace covalente, los electrones son "colaborados", permaneciendo en una órbita compartida que mantiene unidos a los átomos. Estas diferencias fundamentales tienen un impacto significativo en las propiedades macroscópicas de los compuestos que forman.
Más Allá del Iónico y Covalente: El Enlace Metálico
Además de los enlaces iónicos y covalentes, existe un tercer tipo fundamental de unión que da lugar a las propiedades únicas de los metales: el enlace metálico. A diferencia de los enlaces iónicos, donde los electrones se transfieren, y los covalentes, donde se comparten de forma localizada, el enlace metálico implica un "mar de electrones" deslocalizados. Imagina una multitud de átomos metálicos que han cedido sus electrones de valencia, y estos electrones no pertenecen a ningún átomo en particular, sino que se mueven libremente por toda la estructura metálica. Es como una gran fiesta donde los electrones fluyen sin restricciones.
Esta atracción entre los iones metálicos cargados positivamente (los núcleos de los átomos metálicos con sus electrones internos) y el "mar" de electrones deslocalizados es lo que define el enlace metálico. Esta libertad de movimiento de los electrones es la razón por la que los metales son excelentes conductores de electricidad y calor, maleables (pueden ser martillados en láminas) y dúctiles (pueden ser estirados en hilos). A diferencia de los compuestos iónicos, que son frágiles y se rompen, los metales pueden deformarse sin romperse debido a que los iones pueden deslizarse unos sobre otros sin perder el contacto con el mar de electrones.

Impacto en las Propiedades de la Materia
La naturaleza del enlace químico tiene un impacto profundo en las propiedades físicas y químicas de los materiales. Comprender si un compuesto es iónico, covalente o metálico nos permite predecir y explicar muchas de sus características:
- Puntos de Fusión y Ebullición: Los compuestos iónicos, como el cloruro de sodio, tienen puntos de fusión y ebullición muy altos (801 °C y 1413 °C, respectivamente) debido a las fuertes fuerzas electrostáticas que mantienen unidos a los iones en la red cristalina. Se requiere una gran cantidad de energía para superar estas fuerzas. Los compuestos covalentes moleculares, como el agua (0 °C y 100 °C), suelen tener puntos de fusión y ebullición más bajos porque las fuerzas entre las moléculas individuales son mucho más débiles que los enlaces covalentes dentro de las moléculas. Sin embargo, las redes covalentes, como el diamante, tienen puntos de fusión extremadamente altos porque los átomos están unidos por una red continua de enlaces covalentes muy fuertes.
- Conductividad Eléctrica: Los compuestos iónicos no conducen electricidad en estado sólido porque sus iones están fijos en la red cristalina y no pueden moverse libremente. Sin embargo, cuando se funden o se disuelven en agua, los iones se liberan y pueden moverse, lo que les permite conducir la electricidad. Los compuestos covalentes moleculares generalmente no conducen electricidad porque no tienen iones libres ni electrones deslocalizados. Los metales, por otro lado, son excelentes conductores de electricidad y calor debido a su "mar de electrones" móviles.
- Solubilidad: Los compuestos iónicos tienden a ser solubles en disolventes polares como el agua. Las moléculas de agua, que son polares, pueden rodear y separar los iones individuales de la red cristalina, disolviendo el compuesto. Los compuestos covalentes varían en su solubilidad; las moléculas polares son solubles en disolventes polares, mientras que las moléculas apolares son solubles en disolventes apolares (principio de "lo similar disuelve lo similar").
- Dureza y Fragilidad: Los compuestos iónicos son típicamente duros y frágiles. Son duros porque las fuerzas electrostáticas son fuertes, pero frágiles porque si se aplica una fuerza que desplaza los iones, las repulsiones entre iones de la misma carga pueden hacer que la estructura se rompa. Los metales son maleables y dúctiles debido a la naturaleza del enlace metálico que permite que los iones se deslicen sin perder el contacto con el mar de electrones. Los compuestos covalentes varían enormemente, desde gases blandos hasta sólidos extremadamente duros como el diamante.
En esencia, la forma en que los átomos interactúan a nivel electrónico es el lenguaje fundamental que la materia utiliza para expresar sus características. Desde la transparencia del vidrio hasta la conductividad del cobre, cada propiedad es un eco de las fuerzas y los acuerdos a nivel atómico.
Preguntas Frecuentes sobre Enlaces Químicos
¿Qué significa que un enlace sea iónico?
Significa que el enlace se forma por la atracción electrostática entre iones de carga opuesta, los cuales se generan por la transferencia completa de uno o más electrones de un átomo a otro. Un átomo pierde electrones (convirtiéndose en catión positivo) y otro los gana (convirtiéndose en anión negativo).
¿Cuál es la diferencia principal entre un enlace iónico y uno covalente?
La diferencia principal radica en la forma en que se manejan los electrones: en un enlace iónico, los electrones son transferidos completamente de un átomo a otro. En contraste, en un enlace covalente, los electrones son compartidos entre los átomos participantes.
¿Entre qué tipos de átomos se forman los enlaces iónicos?
Los enlaces iónicos se forman generalmente entre átomos de elementos con una gran diferencia de electronegatividad, típicamente entre un metal (que tiende a ceder electrones) y un no metal (que tiende a aceptar electrones).

¿Los compuestos iónicos conducen la electricidad?
Los compuestos iónicos no conducen electricidad en estado sólido porque sus iones están fijos en una red cristalina. Sin embargo, sí conducen electricidad cuando están fundidos o disueltos en agua, ya que en estos estados los iones se vuelven móviles y pueden transportar la carga.
¿Qué diferencia hay entre un enlace iónico y uno metálico?
El enlace iónico implica la transferencia de electrones y la formación de iones discretos que se atraen. El enlace metálico, por otro lado, se caracteriza por la atracción entre iones metálicos positivos y un "mar" de electrones deslocalizados o "libres" que se mueven por toda la estructura, no perteneciendo a ningún átomo en particular.
¿Por qué los compuestos iónicos tienen altos puntos de fusión?
Tienen altos puntos de fusión debido a las muy fuertes fuerzas electrostáticas que existen entre los iones cargados opuestamente. Se requiere una gran cantidad de energía térmica para romper estas fuerzas y permitir que los iones se muevan libremente en el estado líquido.
En resumen, la danza de los electrones es un espectáculo fascinante y fundamental que define la química de nuestro universo. Los enlaces iónicos, con su dramática transferencia de electrones, y los enlaces covalentes, con su armoniosa compartición, son dos de los pilares sobre los que se construye la materia. Junto con el dinámico enlace metálico, estas uniones atómicas no solo explican la existencia de innumerables compuestos, sino que también nos brindan la clave para manipular y crear nuevos materiales con propiedades específicas. Entender estas distinciones no es solo un ejercicio académico, sino una ventana a la complejidad y belleza del mundo a escala atómica.
Si quieres conocer otros artículos parecidos a El Baile de los Electrones: Iónico, Covalente y Más puedes visitar la categoría Metáforas.
