26/10/2015
Desde los primeros pasos de la humanidad en la comprensión de la materia, la búsqueda de modelos visuales ha sido fundamental. Uno de los más persistentes y, a la vez, incompletos, es la comparación del átomo con un sistema solar en miniatura. Esta imagen, donde los electrones giran alrededor de un núcleo como planetas alrededor de una estrella, ha arraigado profundamente en el imaginario colectivo. Es una analogía poderosa por su simplicidad y familiaridad, pero ¿cuánto de verdad hay en ella? Acompáñanos en este viaje para desentrañar por qué esta metáfora, aunque histórica y pedagógicamente útil, se queda corta ante la asombrosa realidad de la mecánica cuántica.
- El Nacimiento de una Idea: El Modelo de Rutherford
- El Avance de Bohr: Cuantización en el Mini Sistema Solar
- Las Limitaciones de la Analogía: ¿Por Qué el Átomo No Es un Sistema Solar?
- El Modelo Cuántico Moderno: Una Realidad Más Compleja
- ¿Por Qué la Analogía Persiste y Es Útil?
- Tabla Comparativa: Átomo vs. Sistema Solar
- Preguntas Frecuentes (FAQ)
- ¿Es el modelo planetario del átomo completamente erróneo?
- ¿Por qué seguimos usando la analogía del sistema solar para explicar el átomo?
- ¿Cómo se describen los electrones en la física moderna si no están en órbitas?
- ¿Qué es un orbital atómico?
- ¿Qué modelo atómico introdujo la idea de órbitas cuantizadas?
- Conclusión
El Nacimiento de una Idea: El Modelo de Rutherford
Para entender por qué la analogía del sistema solar se volvió tan popular, debemos remontarnos a principios del siglo XX, específicamente al trabajo pionero de Ernest Rutherford. Antes de él, el modelo atómico más aceptado era el de J.J. Thomson, conocido como el "pudín de pasas", donde la carga positiva y negativa estaban distribuidas uniformemente. Sin embargo, los experimentos de Rutherford en 1911 cambiarían radicalmente esta visión.
Rutherford y sus colaboradores, Geiger y Marsden, llevaron a cabo el famoso experimento de la lámina de oro. Bombardearon una fina lámina de oro con partículas alfa (núcleos de helio, con carga positiva). Si el modelo del "pudín de pasas" fuera correcto, se esperaría que las partículas alfa pasaran a través de la lámina con apenas una ligera desviación, ya que la carga positiva del átomo estaría muy dispersa. Sin embargo, los resultados fueron sorprendentes: la mayoría de las partículas alfa atravesaron la lámina sin desviarse, pero un pequeño porcentaje se desvió en ángulos muy grandes, e incluso algunas rebotaron hacia atrás.
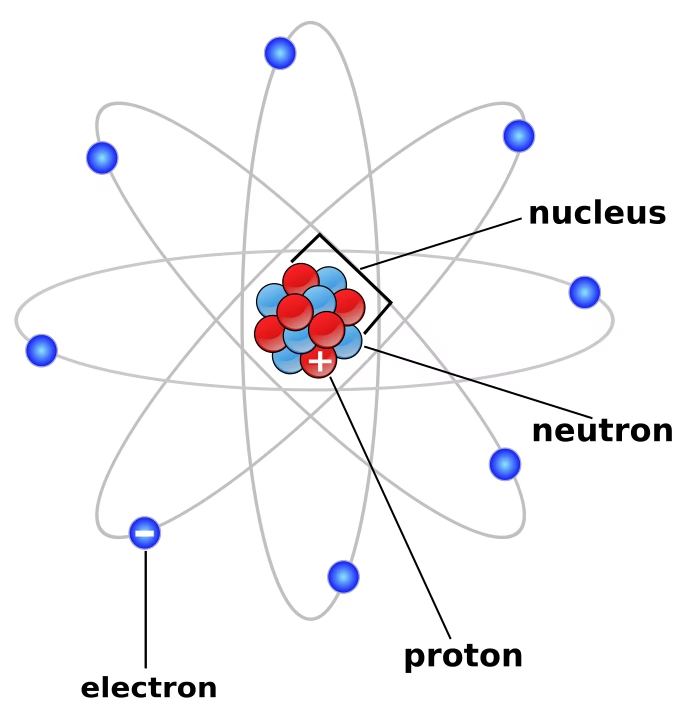
Estos resultados llevaron a Rutherford a una conclusión revolucionaria: la mayor parte de la masa y toda la carga positiva del átomo debían estar concentradas en un espacio extremadamente pequeño en el centro, al que llamó núcleo. Los electrones, mucho más ligeros y con carga negativa, debían estar orbitando alrededor de este núcleo a una gran distancia, en un espacio mayormente vacío. La imagen que emergió de este modelo era, por lo tanto, la de un sistema planetario: un núcleo central (el sol) y electrones girando a su alrededor (los planetas).
Las implicaciones de este modelo eran enormes. Sugería que el átomo era, en su mayor parte, espacio vacío, y que la relación de tamaño entre el núcleo y el átomo era comparable a la de un botón en el centro de una plaza de toros. A pesar de su éxito para explicar los resultados experimentales, el modelo de Rutherford presentaba una seria inconsistencia con la física clásica: según las leyes del electromagnetismo, un electrón que orbita (y por lo tanto, acelera) debería emitir radiación electromagnética y, al perder energía, espiralar rápidamente hacia el núcleo, provocando el colapso del átomo. Claramente, esto no sucede, ya que la materia es estable.
El Avance de Bohr: Cuantización en el Mini Sistema Solar
La estabilidad del átomo fue uno de los grandes misterios que el modelo de Rutherford no pudo resolver. Fue Niels Bohr quien, en 1913, dio un paso crucial para superar esta limitación, adoptando el modelo planetario de Rutherford pero introduciendo conceptos de la entonces naciente mecánica cuántica. El modelo de Bohr, aunque aún concibe el átomo como un pequeño sistema solar, añade reglas específicas para los electrones.
Bohr propuso dos postulados fundamentales:
- Postulado de las Órbitas Estacionarias: Los electrones solo pueden existir en ciertas órbitas específicas, llamadas órbitas estacionarias o niveles de energía, sin emitir ni absorber energía. En estas órbitas, el momento angular del electrón está cuantizado, es decir, solo puede tomar valores que son múltiplos enteros de una constante fundamental (h/2π, donde 'h' es la constante de Planck). Esto resolvió el problema del colapso: mientras el electrón permanezca en una de estas órbitas permitidas, no irradia energía.
- Postulado de la Transición de Energía: Un electrón solo emite o absorbe energía cuando salta de una órbita estacionaria a otra. La energía de la radiación emitida o absorbida es exactamente igual a la diferencia de energía entre las dos órbitas involucradas. Esto explicaba las líneas espectrales discretas que se observaban en los átomos, especialmente en el hidrógeno, un fenómeno que el modelo de Rutherford no podía justificar.
El modelo de Bohr fue un éxito rotundo para explicar el espectro del átomo de hidrógeno y proporcionó una base teórica para la cuantificación de la energía. Aunque seguía siendo un modelo planetario, la introducción de la cuantización de las órbitas y los niveles de energía marcó una diferencia fundamental con la física clásica. Los electrones no podían ocupar cualquier órbita, sino solo aquellas "permitidas", como escalones en una escalera de energía. Este modelo es a menudo el primero que se enseña en las escuelas, dada su simplicidad y su capacidad para introducir conceptos cuánticos básicos de manera intuitiva.
Las Limitaciones de la Analogía: ¿Por Qué el Átomo No Es un Sistema Solar?
A pesar de la brillantez del modelo de Bohr y su capacidad para explicar ciertos fenómenos, pronto se hizo evidente que la analogía del sistema solar, incluso con las modificaciones cuánticas de Bohr, era una simplificación excesiva y, en última instancia, incorrecta para describir la verdadera naturaleza del átomo. Las discrepancias surgieron al intentar aplicarlo a átomos con más de un electrón, así como al explicar fenómenos más complejos como el efecto Zeeman (la división de las líneas espectrales en presencia de un campo magnético).
Las principales razones por las que un átomo no es como un sistema solar son:
- Naturaleza de las Partículas: En un sistema solar, los planetas son objetos macroscópicos con trayectorias bien definidas, gobernadas por las leyes de la gravedad de Newton. En el átomo, los electrones son partículas subatómicas que se rigen por las leyes de la mecánica cuántica. A esta escala, las partículas no tienen una posición y un momento exactos y simultáneos (Principio de Incertidumbre de Heisenberg).
- Órbitas vs. Orbitales: Los planetas tienen órbitas precisas y predecibles. Los electrones, en cambio, no "orbitan" en el sentido clásico. En la mecánica cuántica, la posición de un electrón se describe mediante una función de probabilidad. Esto da lugar al concepto de orbital, que es una región tridimensional alrededor del núcleo donde hay una alta probabilidad de encontrar un electrón. No son trayectorias fijas, sino "nubes" de probabilidad.
- Interacciones Fundamentales: La fuerza que mantiene unidos los sistemas solares es la gravedad, una fuerza relativamente débil pero de largo alcance que actúa sobre grandes masas. En el átomo, la fuerza que une los electrones al núcleo es la fuerza electromagnética, que es mucho más intensa y domina a escala atómica. Si los electrones se comportaran como planetas bajo el electromagnetismo, el átomo colapsaría por radiación, como se mencionó anteriormente. La estabilidad atómica es una propiedad puramente cuántica.
- Vacío Atómico: Aunque ambos son mayormente "espacio vacío", la naturaleza de ese vacío es diferente. En el sistema solar, el espacio entre el sol y los planetas es un vacío casi perfecto. En el átomo, el "vacío" entre el núcleo y el orbital de electrones está lleno de campos cuánticos y potenciales de interacción.
- Energía y Radiación: Los planetas pueden ajustar sus órbitas de manera continua si interactúan con otros cuerpos. Los electrones, según la mecánica cuántica, solo pueden tener valores de energía discretos. No pueden ocupar cualquier nivel de energía, y la transición entre ellos implica la emisión o absorción de paquetes de energía específicos (fotones).
El Modelo Cuántico Moderno: Una Realidad Más Compleja
Las limitaciones del modelo de Bohr y la analogía planetaria impulsaron el desarrollo de la mecánica cuántica en las décadas de 1920 y 1930, con figuras como Erwin Schrödinger, Werner Heisenberg y Paul Dirac. Este nuevo marco teórico revolucionó nuestra comprensión del átomo.
El modelo atómico moderno, basado en la mecánica cuántica, abandona la idea de órbitas definidas y las reemplaza por orbitales atómicos. Estos orbitales son soluciones matemáticas a la ecuación de Schrödinger que describen la distribución de probabilidad de encontrar un electrón en una región específica del espacio alrededor del núcleo. Los electrones se caracterizan por un conjunto de números cuánticos (principal 'n', azimutal 'l', magnético 'm_l' y de espín 'm_s') que describen su energía, la forma de su orbital, su orientación espacial y su espín intrínseco. No se puede predecir la trayectoria exacta de un electrón, solo la probabilidad de encontrarlo en un lugar determinado.

Esta visión es mucho menos intuitiva que la del sistema solar, pero es la que mejor se ajusta a las observaciones experimentales y a la estabilidad de la materia. Es un modelo que desafía nuestra percepción macroscópica y nos introduce en un mundo donde la incertidumbre y la probabilidad son inherentes.
¿Por Qué la Analogía Persiste y Es Útil?
A pesar de sus inexactitudes, la analogía del átomo como un sistema solar se sigue utilizando ampliamente en la enseñanza y la divulgación científica, especialmente en los niveles introductorios. ¿Por qué?
La razón principal es su valor pedagógico. Es una forma sencilla y visual de introducir conceptos complejos a estudiantes que aún no están familiarizados con la abstracción de la mecánica cuántica. Permite:
- Visualizar la idea de un centro denso (núcleo) y partículas más ligeras que lo rodean.
- Comprender que el átomo es mayormente espacio vacío.
- Introducir la noción de que los electrones están en movimiento alrededor del núcleo.
- Servir como un trampolín para modelos más avanzados, demostrando cómo la ciencia evoluciona a medida que se obtiene nueva información.
Es una metáfora que, aunque no sea literalmente correcta, cumple su función de ayudar a construir una comprensión inicial, un punto de partida desde el cual se puede progresar hacia una imagen más precisa y sofisticada del átomo. Es importante, sin embargo, que al presentar esta analogía, se enfatice claramente que es una simplificación y que la realidad cuántica es mucho más profunda y fascinante.
Tabla Comparativa: Átomo vs. Sistema Solar
Para resumir las similitudes y, lo que es más importante, las diferencias, podemos utilizar la siguiente tabla:
| Característica | Átomo (Modelo Moderno) | Sistema Solar |
|---|---|---|
| Cuerpo Central | Núcleo (protones y neutrones) | Sol |
| Cuerpos Orbitantes | Electrones | Planetas, asteroides, cometas |
| Fuerza Dominante | Fuerza Electromagnética (entre núcleo y electrones) | Fuerza Gravitatoria (entre cuerpos masivos) |
| Naturaleza del Movimiento | Cuántico (probabilístico, descrito por orbitales) | Clásico (determinista, trayectorias definidas) |
| Estabilidad | Estable debido a la cuantización de energía (mecánica cuántica) | Estable por equilibrio gravitatorio y velocidad tangencial |
| Tamaño Relativo | Núcleo ~100.000 veces más pequeño que el átomo | Sol mucho más grande que los planetas, pero el espacio entre ellos es vasto |
| Capacidad de Radiar | Solo al saltar entre niveles de energía discretos | Continuamente (pero insignificante para planetas) si aceleran, colapsaría si fuera electromagnético |
| Escala | Microscópica (nanómetros y picómetros) | Macroscópica (millones a miles de millones de kilómetros) |
Preguntas Frecuentes (FAQ)
¿Es el modelo planetario del átomo completamente erróneo?
No es completamente erróneo en su concepto básico de un núcleo central y electrones que lo rodean, pero es una simplificación importante. El modelo de Rutherford fue un avance crucial, y el de Bohr añadió la importantísima idea de la cuantificación de la energía. Sin embargo, ambos modelos tienen limitaciones significativas y no describen con precisión el comportamiento de los electrones a nivel cuántico. El modelo moderno de la mecánica cuántica es el que ofrece la descripción más precisa y completa.
¿Por qué seguimos usando la analogía del sistema solar para explicar el átomo?
La analogía persiste por su gran valor pedagógico y su facilidad para visualizar una estructura compleja e invisible. Permite a los estudiantes y al público en general formarse una imagen inicial intuitiva de un núcleo central y partículas más pequeñas que lo rodean, así como la idea de que el átomo es mayormente espacio vacío. Es un punto de partida útil antes de introducir conceptos más abstractos de la mecánica cuántica.
¿Cómo se describen los electrones en la física moderna si no están en órbitas?
En la física moderna, basada en la mecánica cuántica, los electrones se describen mediante funciones de onda que definen orbitales. Un orbital no es una trayectoria fija, sino una región tridimensional alrededor del núcleo donde la probabilidad de encontrar un electrón es alta. Los electrones no tienen una posición y un momento definidos simultáneamente (Principio de Incertidumbre de Heisenberg), y su comportamiento es probabilístico, no determinista como el de los planetas.
¿Qué es un orbital atómico?
Un orbital atómico es una región del espacio alrededor del núcleo donde existe una alta probabilidad (generalmente el 90-95%) de encontrar un electrón con una energía y propiedades específicas. Cada orbital tiene una forma y una orientación espacial características (esférica para los orbitales 's', en forma de mancuerna para los 'p', etc.) y puede albergar un máximo de dos electrones con espines opuestos.
¿Qué modelo atómico introdujo la idea de órbitas cuantizadas?
Fue el modelo atómico de Niels Bohr, propuesto en 1913, el que introdujo la idea revolucionaria de que los electrones solo pueden existir en órbitas específicas y discretas, o niveles de energía, sin emitir energía. Esta cuantización de las órbitas fue fundamental para explicar la estabilidad de los átomos y los espectros de emisión y absorción.
Conclusión
La analogía del átomo como un sistema solar es una metáfora poderosa que ha servido como un puente crucial en nuestra comprensión de la materia. Desde los hallazgos de Rutherford que revelaron el núcleo denso y el vasto espacio vacío del átomo, hasta las correcciones de Bohr que introdujeron la cuantización de la energía, esta imagen ha sido fundamental en la evolución de la química y la física. Sin embargo, es vital reconocer que, como toda analogía, tiene sus límites. La verdadera naturaleza del átomo reside en el fascinante y a menudo contraintuitivo reino de la mecánica cuántica, donde los electrones no son pequeños planetas que giran en órbitas definidas, sino entidades probabilísticas que habitan en "nubes" llamadas orbitales.
Entender esta distinción no solo enriquece nuestra visión de la ciencia, sino que también nos invita a apreciar la complejidad y la belleza de un universo que opera bajo reglas que van más allá de nuestra experiencia cotidiana. La analogía del sistema solar sigue siendo una excelente herramienta para iniciar el viaje, pero es solo el primer paso hacia una comprensión más profunda y asombrosa de la realidad atómica.
Si quieres conocer otros artículos parecidos a Átomos y Sistemas Solares: Una Metáfora Incompleta puedes visitar la categoría Metáforas.

